EBV R-GENE®
Trousse de PCR* en temps réel pour une détection et une quantification de l’ADN du virus d’Epstein-Barr (EBV)
- Quantification précise de la charge virale de l’EBV sur une large gamme de linéarité
- Réactifs prêts à l’emploi comprenant le contrôle interne et les standards de quantification
- CE-IVD sur différents types d’échantillons ainsi que sur l'ensemble des principales plates-formes d’extraction et les systèmes de PCR en temps réel
Ajouter à ma sélection
Avez-vous besoin de plus d'informations?
Application Clinique
Mars 2016
Avantages de EBV R-gene®
Le virus d’Epstein-Barr (EBV), connu comme l’agent étiologique de la mononucléose infectieuse, est responsable de la lymphoprolifération des cellules B (syndrome lymphoprolifératif (SLP) post-transplantation, lymphome de Burkitt, lymphome de Hodgkin…), une complication grave chez les patients immunodéprimés. Il est essentiel d’optimiser la détection et le suivi de l’infection à EBV afin d’assurer une meilleure prise en charge du patient. EBV R-gene® offre une détection rapide et spécifique d'EBV avant l’apparition des signes cliniques. Pendant le traitement, les mesures de la charge virale et de sa cinétique sont des indicateurs de l’efficacité du traitement.
Après le traitement, le suivi de la charge virale peut être utile au décours du traitement pour dépister une éventuelle rechute.
En outre, pour plus d'efficacité, vous pouvez utiliser la gamme exhaustive R-gene® pour quantifier différents virus à partir d’un même échantillon ou analyser simultanément plusieurs échantillons pour détecter le même virus.
- Sensible et reproductible
- Mesure fiable de l’infection à EBV
- Large gamme de linéarité
-
Standardisé
- Traitement uniforme de plusieurs analyses grâce à la gamme de produits R-gene® (CMV R-gene®, HSV1 HSV2 VZV R-gene®, CMV HHV6,7,8 R-gene®, BK Virus R-gene®, Adenovirus R-gene®, Parvovirus B19 R-gene®)
-
Profils de tests harmonisés pour procéder simultanément à plusieurs essais
-
Protocole de conversion des résultats quantitatifs en UI/mL, tel que défini dans le premier standard international de l’OMS
- Flexible
- Trousse validée pour une utilisation avec différents types d’échantillons
-
Préparation des échantillons manuelle ou automatisée tel que sur NucliSENS® easyMAG®
- Préparation des réactions PCR* manuelle ou automatisée par le robot de pipettage easySTREAM®™
-
Trousse qualifiée pour les principales plates-formes de PCR en temps réel
Tout ce dont vous avez besoin dans une seule trousse
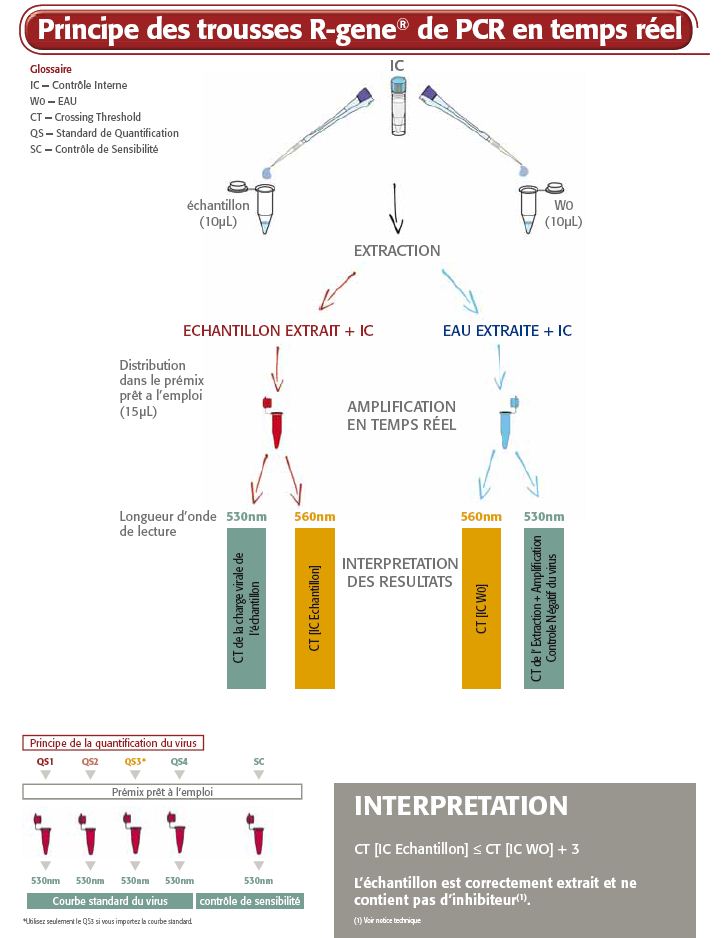
La trousse de détection moléculaire EBV R-gene® prête à l’emploi permet de mesurer la charge virale de l’EBV dans des extraits d’ADN issus de différents échantillons cliniques. Ce test de PCR en temps réel basé sur la technologie 5' nucléase Taqman amplifie une région spécifique du génome EBV pour la détection et la quantification de l'EBV.
- Quatre standards de quantification permettent de mesurer précisément la charge virale de l’EBV
- Un contrôle de sensibilité valide les performances du test
- Un contrôle interne (IC2) vérifie le processus d’extraction, dès l’étape de lyse, et la présence d’inhibiteurs d’amplification dans l’échantillon
-
Tous les réactifs nécessaires optimisés pour détecter et quantifier le virus EBV à des fins de diagnostic in vitro sont prêts à l’emploi :
- Réduction du temps de préparation
- Réduction des risques d’erreur de manipulation ou de dilution
-
Réduction du risque de contamination
Une procédure facile
Grâce à la trousse EBV R-gene®, il suffit d’ajouter l’ADN extrait de l’échantillon au prémix d'amplification PCR* prêt à l’emploi et de commencer la réaction sur le thermocycleur de PCR* en temps réel approprié, en suivant le programme de cycles optimisé décrit dans les « Instructions d’utilisation » de la Notice Technique.
*PCR = Polymerase Chain Reaction (en français Réaction en Chaine par polymérase)
BIOMERIEUX, le logo bleu, ARGENE®, R-gene®, EASYMAG® et NUCLISENS® sont des marques utilisées, déposées et/ou enregistrées appartenant à bioMérieux, ou à l’une de ses filiales, ou à l’une de ses sociétés. Les autres marques et noms de produits mentionnés appartiennent à leurs propriétaires respectifs.
BIOMERIEUX, the blue logo, ARGENE®,R-gene®, EASYMAG® and NUCLISENS® are used, pending and/or registered trademarks belonging to bioMérieux, or one of its subsidiaries, or one of its companies.
Any other name or trademark is the property of its respective owner. - See more at: http://clinical.biomerieux.net/cmv-r-gene-0#sthash.YR9WVorN.dpuf
Any other name or trademark is the property of its respective owner. - See more at: http://clinical.biomerieux.net/cmv-r-gene-0#sthash.YR9WVorN.dpuf
BIOMERIEUX, the blue logo, ARGENE®,R-gene®, EASYMAG® and NUCLISENS® are used, pending and/or registered trademarks belonging to bioMérieux, or one of its subsidiaries, or one of its companies.
Any other name or trademark is the property of its respective owner. - See more at: http://clinical.biomerieux.net/cmv-r-gene-0#sthash.YR9WVorN.dpuf
Any other name or trademark is the property of its respective owner. - See more at: http://clinical.biomerieux.net/cmv-r-gene-0#sthash.YR9WVorN.dpuf
BIOMERIEUX, the blue logo, ARGENE®,R-gene®, EASYMAG® and NUCLISENS® are used, pending and/or registered trademarks belonging to bioMérieux, or one of its subsidiaries, or one of its companies.
Any other name or trademark is the property of its respective owner. - See more at: http://clinical.biomerieux.net/cmv-r-gene-0#sthash.YR9WVorN.dpuf
Any other name or trademark is the property of its respective owner. - See more at: http://clinical.biomerieux.net/cmv-r-gene-0#sthash.YR9WVorN.dpuf
Application Clinique
Mars 2016
| EBV R-GENE® (69-002B) | |
|---|---|
| Principe du test | Détection et quantification du génome d'EBV |
| Références de commande | Référence 69-002B : Trousse de quantification EBV R-gene®. Également disponible sous la référence 69-002 : Trousse COMPLETE (comprenant la trousse de quantification réf. 69-002B et la trousse d’extraction d’ADN réf. 67-000) |
| Technologie | PCR en temps réel. Technologie des sondes d’hydrolyse 5’ nucléase Taqman |
| Gène cible | Région du gène BXLF1 codant pour la thymidine kinase |
| Échantillon*** | Sang total, plasma, liquide céphalorachidien, biopsies, LBA |
| Limite de détection | Sur matrice sang total : LoD** 95% : 182 copies/mL 4 copies/PCR |
| Contrôles inclus | Contrôle d’extraction + inhibition, contrôle de sensibilité, contrôle négatif |
| Délai d’obtention des résultats | 75 minutes (étape d’extraction exclue) |
| Unité de mesure | Copies/mL ou conversion en UI/mL tel que défini dans le premier standard international de l’OMS |
| Nombre de tests | 90 tests |
| Conditions de conservation | -18 °C/-22 °C pour la référence 69-002B (Trousse de quantification), +2 °C/+8 °C pour la réf. 67-000 (Trousse d’extraction ADN) |
| Extraction validée*** manuelle ou automatisée |
- MagNA Pure Compact Instrument
- MagNA Pure LC Instrument
- NucliSENS® easyMAG®
- QIAsymphony SP
- QIAamp DNA Blood Mini Kit
- QIAcube
- m2000sp
- Versant kPCR Molecular System SP
- BioRobot EZ1
|
| Plate-forme d’amplification validée*** |
- LightCycler 1.0, 2.0, 480 (System II)
- Applied Biosystems 7000, 7300, 7500, 7500 Fast, 7500 Fast Dx, StepOne, ViiA™7 Real-Time PCR System (avec bloc pour plaques
96 puits et bloc pour plaques 96 puits Fast)
- SmartCycler 2.0
- Rotor-Gene (barrettes PCR de 4 tubes)
- Mx3000P/Mx3005P(Stratagene, Agilent) et Versant kPCR Molecular System AD
- Dx Real-Time System et CFX96 Real Time System
|
| Statut | A utiliser pour le diagnostic in vitro |
**LoD = Limit of detection (en français limite de détection)
***Veuillez vous renseigner
Application Clinique
Mars 2016
Quelques informations sur l’EBV
Qu’est-ce que l’EBV ?
Le virus d’Epstein-Barr (EBV) est un herpèsvirus ubiquitaire qui infecte la majorité de la population humaine. A la suite de la primo-infection (transmission par l’intermédiaire de la salive), l’EBV persiste à l’état latent dans les lymphocytes B. Des épisodes de réactivation peuvent survenir occasionnellement chez les individus immunocompétents, caractérisés par une réplication de l’EBV dans l’oropharynx, sans signe clinique associé.
Population à risque
L’EBV est l'agent causal de la mononucléose infectieuse (MNI) et il est impliqué dans la pathogénie de plusieurs cancers tels que le lymphome de Burkitt, le lymphome de Hodgkin et le carcinome du nasopharynx. Chez les individus immunodéprimés, la prolifération non contrôlée de lymphocytes B infectées par l’EBV peut également entraîner un syndrome lymphoprolifératif (SLP) post-transplantation, cause importante de morbidité et de mortalité chez les patients ayant reçu une greffe d’organe et les patients ayant reçu une greffe de cellules souches hématopoïétiques (GCSH).
Quels sont les avantages du test moléculaire EBV ?
Les essais basés sur la PCR en temps réel pour EBV permettent une détection rapide et spécifique avant l’apparition de symptômes cliniques afin d’améliorer les résultats. Cela est spécialement important pour les patients immunodéprimés chez qui l’infection peut avoir des conséquences particulièrement graves. La PCR en temps réel pour la détection quantitative de l’EBV peut être utilisée pour aider au diagnostic précoce du SLP, suivre l’évolution de la maladie et surveiller la réponse au traitement.
EBV R-gene® et le premier standard international de l’OMS pour le virus d’Epstein-Barr (EBV)
Vous avez besoin de calculer votre facteur de conversion pour exprimer vos résultats EBV R-gene® en UI/mL ?
R-gene®: PUBLICATIONS
- Evaluation of the Epstein-Barr virus R-gene quantification kit in whole blood with different extraction methods and PCR platforms
Fafi-Kremer et al.
J Mol Diagn. 2008 Jan;10(1):78-84. Epub 2007 Dec 28
- Measurement of HSV1, CMV, HHV6 and EBV viral loads in 83 bronchoalveolar lavage (BAL) from lung transplant recipients.
Germi et al.
Unit of Virus Host Cell Interactions, Grenoble
ESCV 2011
- Evaluation de la trousse EBV R-gene (Argene) : Mesure de la charge virale EBV dans des prélèvements de sang total et dans les échantillons du panel européen QCMD
Brunet et al.
Service de virologie, Groupe Hospitalier Pitié-Salpêtrière, AP-HP, Paris
RICAI 2010
- Intérêt de la PCR quantitative EBV dans le suivi des greffés de moelle osseuse en pédiatrie
Billaud et al.
Laboratoire de Virologie, Hopital Debrousse, Lyon.
RICAI
- Comparative evaluation of the NucliSENS® easyMAG™ automated system for the extraction of viral DNA from whole blood samples: application to the monitoring of cytomegalovirus (CMV) and Epstein-Barr virus (EBV) loads
Pillet et al
Laboratoire de Bacteriologie-Virologie-Hygiène, Hopital Nord, CHU de Saint-Etienne, France.
ECCMID 2008
- Clinical and Laboratory Evaluation of the new Argene EBV DNA quantitative real-time PCR assay (R-gene)
Laura Jane Scott et al
West Scotland Specialist Virology Centre, Gartnavel General Hospital, Glasgow, Scotland.
International Symposium on molecular diagnostics, 2006