Parvovirus B19 R-GENE®
Real-Time PCR Kit für den Nachweis und die Quantifizierung von Parvovirus B19 DNA
- Genaue und gleichzeitige Quantifizierung von 3 Parvovirus B19 Genotypen über einen breiten linearen Messbereich
- Gebrauchsfertiger Kit inklusive interner Kontrolle und Quantifizierungsstandards
- CE-IVD zugelassen für alle wichtigen Extraktionsplattformen und Real-Time PCR Systeme sowie für verschiedene Probenarten
Benötigen Sie weitere Informationen?
Vorteile von Parvovirus B19 R-GENE®
Infektionen mit Parvovirus B19 können bei gefährdeten Personen (Schwangere, Patienten mit angeborener Anämie) oder immunsupprimierten Patienten (wie Transplantatempfänger, AIDS Patienten, etc.) schwerwiegende Folgen haben. Ein optimierter Nachweis von Parvovirus B19 ist deshalb wichtig. Parvovirus R-GENE® ist die ideale Lösung für einen schnellen und spezifischen Nachweis und die Quantifizierung der drei Parvovirus B19 Genotypen. Noch mehr Effizienz können Sie erzielen, wenn Sie mit der umfassenden R-GENE® Produktpalette verschiedene Erreger in einer Probe nachweisen oder mehrere Proben gleichzeitig auf ein Virus testen.
- Empfindlich und reproduzierbar
- Zuverlässiger Nachweis einer Parvovirus Infektion
- Breiter linearer Messbereich
- Standardisiert
- Gleichzeitige Durchführung mit Tests der R-GENE® (CMV R-GENE®, EBV R-GENE®, HSV1 HSV2 VZV R-GENE®, CMV HHV6,7,8 R-GENE®, BK Virus R-GENE®, ADENOVIRUS R-GENE®, CMV R-GENE®)
- Einheitliche Testprotokolle für verschiedene Tests in einem Lauf
- Protokoll zur Umrechnung der Quantifizierungsergebnisse in IU/ml mit Hilfe des 1. Intenationalen WHO Standards
- Flexibel:
- Für zahlreiche Probenarten validiert
- Verarbeiten Sie Ihre Proben manuell oder mit automatisierten Plattformen wie dem NucliSENS® easyMAG® oder demeasySTREAM™* Pipettiersystem
- Für alle relevanten Real-Time PCR Plattformen qualifiziert
*Coming soon
Alle Reagenzien in einem Kit
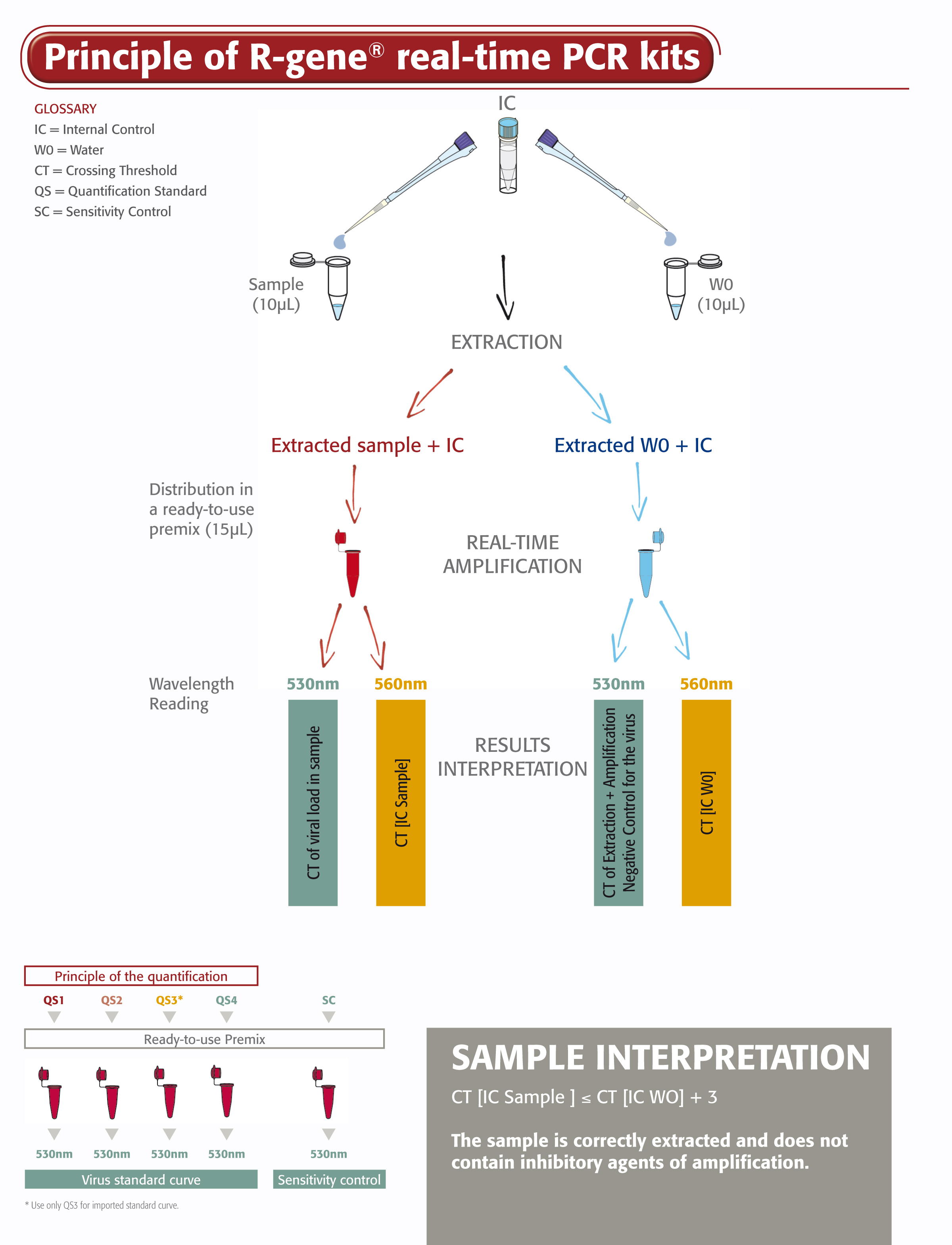
Parvovirus B19 R-GENE® ist ein gebrauchsfertiger molekularbiologischer Kit zum Nachweis und zur Quantifizierung der Viruslast von Parvovirus B19 mittels Real-Time PCR nach Extraktion der DNA aus Vollblut, Plasma und Serum. Dieser Test ermöglicht auch den qualitativen Nachweis aus Knochenmark und medullärem Plasma. Der Test basiert auf der Amplifikation und dem Nachweis einer spezifischen Region des Parvovirus B19 Genoms mittels der 5’ Nuclease TaqMan Technologie.
- Vier Quantifizierungsstandards ermöglichen eine genaue Bestimmung der Parvovirus B19 Viruslast
- Die Sensitivitätskontrolle stellt die Leistungsfähigkeit des Tests sicher
- Eine Interne Kontrolle (IC2) prüft den Extraktionsprozess, einschließlich der Lyse und das Vorliegen von Amplifikationsinhibitoren in der Probe
- Enthält alle erforderlichen Reagenzien für einen optimierten Nachweis und die Quantifizierung von Parvovirus B19 im Rahmen der in vitro Diagnostik
Einfaches Verfahren
Der Parvovirus B19 R-GENE® Kit ist benutzerfreundlich. Einfach die extrahierte DNA zu dem gebrauchsfertigen PCR Master-Mix geben, die Reaktion auf dem entsprechenden Real-Time PCR Thermocycler starten und anschließend das in der Gebrauchsanweisung beschriebene optimierte Cycling Programm durchführen.
BIOMERIEUX, das blaue Logo, ARGENE®, R-GENE®, EASYMAG® und NUCLISENS® sind verwendete, angemeldete und/oder eingetraGENE Marken von bioMérieux, einer ihrer Niederlassungen oder eines ihrer Unternehmen.
Alle anderen Marken und Produktnamen sind Eigentum ihrer jeweiligen Besitzer.
| Parvovirus B19 R-GENE® (69-019B) | |
|---|---|
| Testprinzip | Nachweis und Quantifizierung des Parvovirus B19 Genoms |
| Bestellinformationen | Referenz 69-019B: Parvovirus B19 R-GENE® Kit für den Nachweis und die Quantifizierung. Ebenso erhältlich unter der Referenz 69-019: Komplett-Kit für den Nachweis und die Quantifizierung (enthält den Kit 69-019B für den Nachweis und die Quantifizierung und den DNA Extraktionskit, Ref. 67-000) |
| Technologie | Real-Time PCR / 5‘ Nuclease Taqman Technologie |
| Target-Gen | Gen NS1 |
| Proben* | Vollblut, Plasma, Serum, Knochenmark, medulläres Plasma |
| Nachweisgrenze | Vollblut: 47 Kopien/ml Plasma: 70 Kopien/ml |
| Dynamischer Messbereich | Für die Plasmamatrix: zwischen 5,05 x 1010 Kopien/ml (d.h. 10,7 log10 Kp/ml) und 87 Kopien/ml (d.h. 1,96 log10 Kp/ml). Für die Vollblutmatrix: zwischen 6,1 x 1010 Kopien/ml (d.h. 10,7 log10 Kp/ml) und 42 Kopien/ml d.h. 1,61 log10 Kp/ml) |
| Im Kit enthaltene Kontrollen | Extraktions + Inhibitionskontrolle, Sensitivitätskontrolle, Negativkontrolle |
| Zeit bis zum Vorliegen des Ergebnisses | 75 Minuten (nach dem Extraktionsschritt) |
| Einheit | Kopien/ml – IU/ml (mit dem internatonalen WHA Parvovirus B19 Standard) |
| Anzahl Tests | 90 Tests |
| Lagerungsbedingungen | -18°C/-22°C for reference 69-019B (Detection and Quantification Kit), +2°C/+8°C for ref. 67-000 (DNA Extraction kit) |
| Validierte Extraktionsplattform* Manuell Automatisiert | QIAamp DNA Blood Mini kit NucliSENS® easyMAG® MagNA Pure Compact MagNA Pure LC EZ1 Advanced XL |
| Validierte Amplifikationsplattform* | Life Technologies (ABI7500, ABI7500 Fast & StepOne) LightCycler 2.0 LightCycler 480 System II SmartCycler 2.0 Rotor GENE Q and Rotor GENE 6000 DX Real-Time System CFX96 |
| Status | Für die in vitro Diagnostik, CE Kennzeichnung in Europa - Bitte anfragen |
„Fast Facts“ zu Parvovirus B19
Was ist Parvovirus B19?
Parvovirus B19 gehört zur Familie der Parvoviridae. Aufgrund seiner Struktur und seiner Fähigkeit, die Vorläuferzellen der Erythrozyten zu infizieren, wird es der Gattung Erythrovirus zugeordnet. Es handelt sich um ein nicht umhülltes, einzelsträngiges DNA-Virus von etwa 5,5 kb, welches in drei Genotypen unterteilt werden kann. Am häufigsten tritt der Genotyp 1 auf, der weltweit verbreitet ist, während die Genotypen 2 und 3 eher geographisch begrenzt (Westeuropa, USA, Brasilien und Afrika) und mit niedrigerer Prävalenz auftreten. Parvovirus B19 wird vor allem über Aerosole und Sekrete der Atemwege übertragen.
Welche Personen sind am meisten gefährdet?
Die Erstinfektion erfolgt im Allgemeinen in der Kindheit, obwohl auch Erwachsene von dieser Infektion betroffen sind. Epidemien brechen im Allgemeinen in Schulen und zu bestimmten Jahreszeiten aus, vor allem im Frühjahr und im Winter. Obwohl sich die Infektion meist asymptomatisch zeigt, kann sich die Primärinfektion in Form eines gutartigen Hautausschlages, dem sogenannten Erythema infectiosum (oder Fünfte Krankheit), manifestieren. Das Virus führt auch zu Arthropathien, dem häufigsten Symptom bei infizierten Erwachsenen. Bei gefährdeten oder immunsupprimierten Patienten kann die Infektion schwere Folgeerkrankungen nach sich ziehen. Bei Schwangeren kann eine Primärinfektion zu einer fetalen Anämie führen, die einen Hydrops fetalis, Spontanaborte oder den intrauterinen Fruchttod zur Folge haben kann. Bei Personen mit konstutioneller hämolytischer Anämie kann es Auslöser aplastischer Krisen sein. Bei immunsupprimierten Patienten wie AIDS oder transplantierte Patienten kann es eine schwere chronische Anämie mit Zerstörung der Erythroblasten im Knochenmark hervorrufen. Darüber hinaus wird das Virus mit Herzerkrankungen (Myocarditis) und neurologischen Erkrankungen assoziiert.
Welche Vorteile bietet die molekularbiologische Parvovirus B19 Testung?
Die auf der Real-Time PCR Technologie basierten Parvovirus B19 Tests ermöglichen einen schnellen und spezifischen Nachweis des Virus und tragen somit zu einer Verbesserung des Behandlungserfolgs bei. Mit diesem Test können Sie die Wirksamkeit der aktiven Therapie kontrollieren und Rückfälle nach der Therapie überwachen.
Parvovirus B19 R-GENE® und der Internationale WHO Standard für Parvovirus B19
Sie wollen Ihren Umrechungsfaktor berechnen, um Ihre Parvovirus R-GENE® Ergebnisse in IU/ml anzugeben?
Parvovirus B19 R-GENE®: POSTERS
- Development of a new diagnostic tool for the detection and quantification of Parvovirus B19 by Real Time PCR
Patricia Marechal et al. bioMérieux. ECV 2013 - Evaluation Of a Novel Real Time PCR Assay For Parvovirus B19 (B19V) Genome Detection And Quantification
Aurélie Schnuriger et al. Bacteriology-Virology laboratory, AP-HP Hôpital Trousseau Paris- France. ECV 2013